我們輔導的客戶


暐世生技血糖測試儀 玉美生技器械消毒液
%20(003).jpg)

東研IVD 笠康醫用口罩
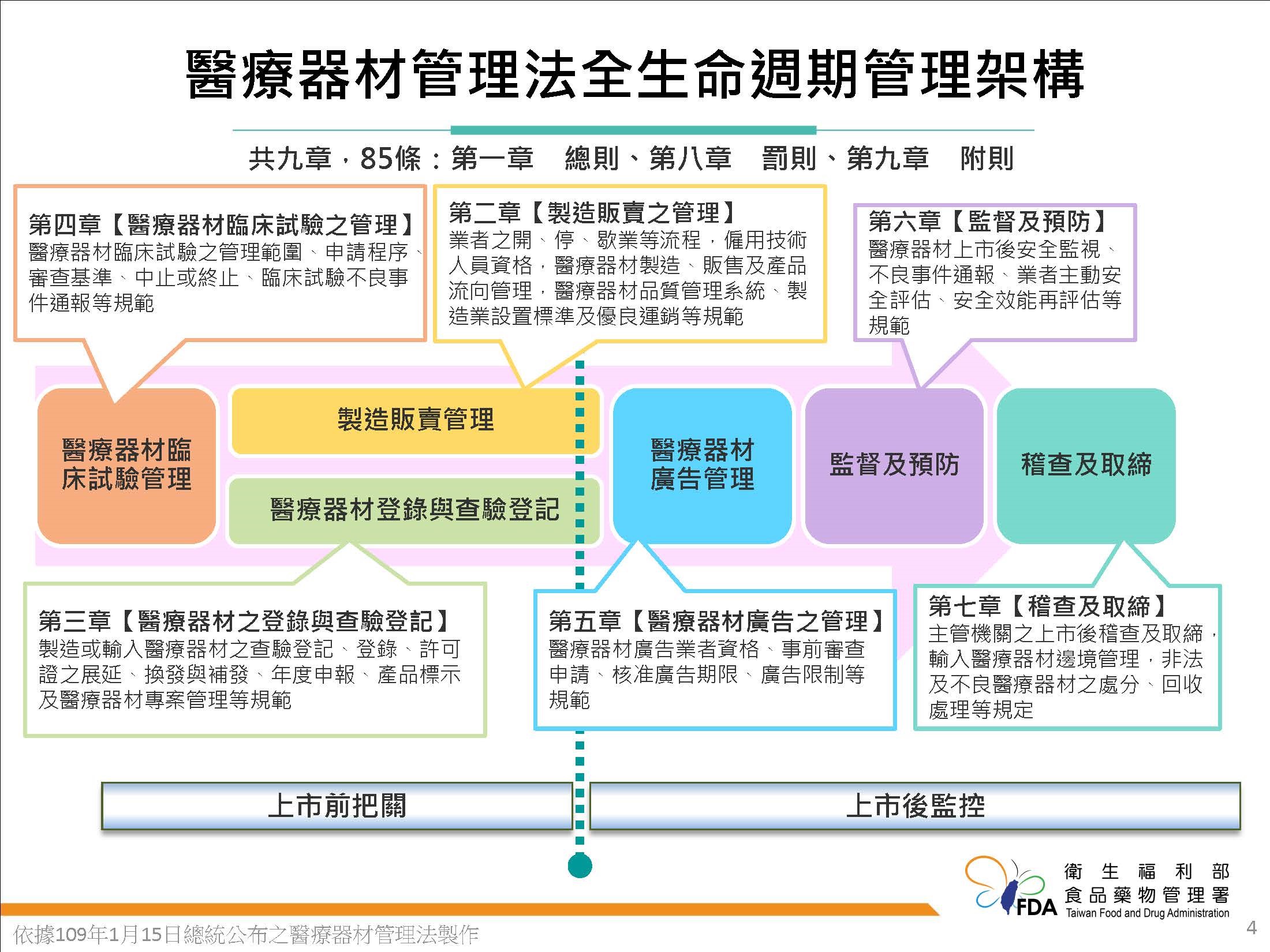
因應醫療器材產品之開發與種類多元化發展,加上醫療器材業者經營管理模式皆與藥品迥然不同,食藥署為健全國內醫療器材管理制度,以及因應國際醫療器材管理法規快速變化趨勢,食藥署歷經多年努力,將醫療器材的管理從「藥事法」中抽離,獨立立法,完成制定「醫療器材管理法」。醫療器材管理法自110年5月1日起施行,法案條文共85條。醫療器材定義
醫療器材管理法第 3 條
醫療器材管理法第 3 條
本法所稱醫療器材,指儀器、器械、用具、物質、軟體、體外診斷試劑及其相關物品,其設計及使用係以藥理、免疫、代謝或化學以外之方法作用於人體,而達成下列主要功能之一者:
一、診斷、治療、緩解或直接預防人類疾病。
二、調節或改善人體結構及機能。
三、調節生育。
前項醫療器材之分類、風險分級、品項、判定原則及其他相關事項之辦法,由中央主管機關定之。
第一項第二款屬非侵入性、無危害人體健康之虞及使用時毋需醫事人員協助之輔具,得報請中央主管機關核准,免列為前項醫療器材之品項。
前項輔具係指協助身心障礙者改善或維護身體功能、構造,促進活動及參與,或便利其照顧者照顧之裝置、設備、儀器及軟體等產品。
一、診斷、治療、緩解或直接預防人類疾病。
二、調節或改善人體結構及機能。
三、調節生育。
前項醫療器材之分類、風險分級、品項、判定原則及其他相關事項之辦法,由中央主管機關定之。
第一項第二款屬非侵入性、無危害人體健康之虞及使用時毋需醫事人員協助之輔具,得報請中央主管機關核准,免列為前項醫療器材之品項。
前項輔具係指協助身心障礙者改善或維護身體功能、構造,促進活動及參與,或便利其照顧者照顧之裝置、設備、儀器及軟體等產品。
醫療器材管理法架構
QMS法源

QMS法源
>醫療器材管理法第 22 條
醫療器材製造業者應建立醫療器材品質管理系統,就場所設施、設備、組織與人事、生產、品質管制、儲存、運銷、客戶申訴及其他事項予以規範,並應符合品質管理系統準則。
醫療器材製造業者依前項準則規定建立醫療器材品質管理系統,並報中央主管機關檢查合格取得製造許可後,始得製造。但經中央主管機關公告之品項,免取得製造許可。
>QMS準則共七章79條,標準模式為第二章至第六章,精要模式為第78條要求
哪些醫療器材製造業者可以申請QMS?
1.醫療器材製造、包裝、貼標、滅菌或最終驗放之業者。
2.醫療器材設計,並以其名義於市場流通之業者。
QMS實施時程
1.自110年05月01日起,新申請案皆須符合QMS準則,並以QMS提出申請。
2. 既有醫療器材製造業者至遲應於113年04月30日前全面符合並取得QMS製造許可。
醫療器材的功能與分級
>醫療器材就其功能、用途、使用方法及工作原理,分類如下
一、臨床化學及臨床毒理學。
二、血液學、病理學及基因學。
三、免疫學及微生物學。
四、麻醉科學。
五、心臟血管醫學科學。
六、牙科學。
七、耳鼻喉科學。
八、胃腸病科學及泌尿科學。
九、一般、整形外科手術及皮膚科學。
十、一般醫院及個人使用裝置。
十一、神經科學。
十二、婦產科學。
十三、眼科學。
十四、骨科學。
十五、物理醫學科學。
十六、放射學科學。
>醫療器材,依其風險程度,分級如下:
一、第一等級:低風險性。
二、第二等級:中風險性。
三、第三等級:高風險性。
醫療器材的功能與分級
>醫療器材就其功能、用途、使用方法及工作原理,分類如下
一、臨床化學及臨床毒理學。
二、血液學、病理學及基因學。
三、免疫學及微生物學。
四、麻醉科學。
五、心臟血管醫學科學。
六、牙科學。
七、耳鼻喉科學。
八、胃腸病科學及泌尿科學。
九、一般、整形外科手術及皮膚科學。
十、一般醫院及個人使用裝置。
十一、神經科學。
十二、婦產科學。
十三、眼科學。
十四、骨科學。
十五、物理醫學科學。
十六、放射學科學。
>醫療器材,依其風險程度,分級如下:
一、第一等級:低風險性。
二、第二等級:中風險性。
三、第三等級:高風險性。
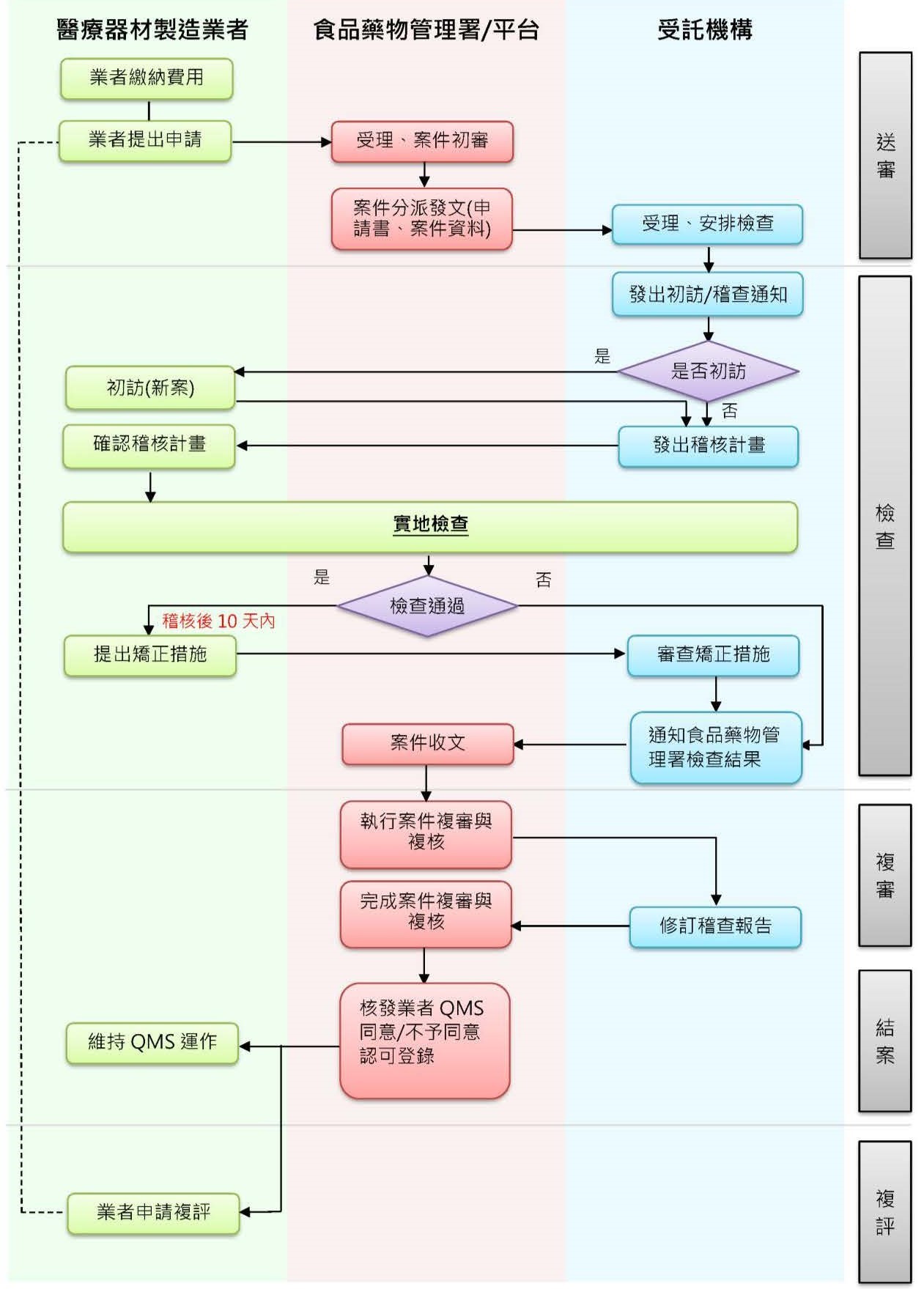
QMS申請查核流程